中国科学技术大学田长麟教授研究组与德国莱布尼茨分子药物所Adam Lange及孙涵课题组合作,应用固体核磁共振、单通道电生理及分子动力学模拟等方法揭示了NaK离子通道的离子选择性新机制。该研究成果以 A single NaK channel conformation is not enough for non-selective ion conduction 为题,于2月19日发表在Nature communications上。
离子通道是细胞膜上的一类特殊亲水性蛋白质微孔道,在细胞膜上形成动作电位和梯度电位,决定细胞的兴奋性和传导性。绝大多数离子通道对不同的离子(K+, Na+, Ca2+, Cl-等)有选择性的通透,但仍有一部分离子通道可以非选择性的通过几种离子。研究人员在KcsA钾离子通道结构基础上,提出了“钾离子通道通过选择过滤器(Selective filter)中主链C=O形成水合离子配位方式实现离子选择性”的静态机制模型,获得了广泛认同。但是,近年来高分辨率X-射线晶体结构显示NaK离子通道在结合不同离子时(如 Na+, K+, Rb+)其静态通道结构完全一致,这无法解释其如何识别和通透这些离子。
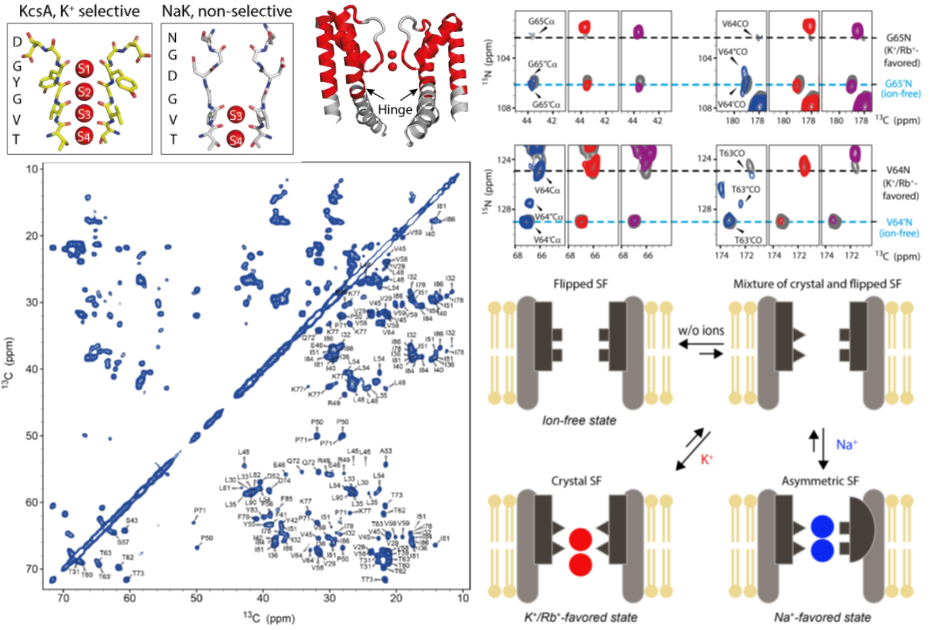
田长麟课题组以非选择性通道NaK为研究对象,将其重组装到磷脂双分子膜内(还原离子通道所存在的细胞膜环境),并与Adam Lange组合作,通过魔角旋转固体核磁方法获得高分辨固体NMR谱图,并获得了不同金属阳离子条件下谱峰归属。NMR谱图数据表明,NaK在生理环境下通道存在两种构象,钾离子选择结合其中一种,而钠离子选择另一种。双方进一步通过固体核磁对原子间距离测量勾画出了两种构象的结构差别,并用分子动力学模拟的方法验证了两种构象分别对K+和Na+有高度的选择性。这一研究成果显示蛋白质构象多样性和构象间的转换对蛋白质功能的重要性,提出了离子通道选择性的新机制。
田长麟教授课题组已毕业博士研究生史朝为、何垚,以及Adam Lange组的博士生Kitty Hendriks为该论文的共同第一作者。该研究得到了基金委、科技部、中科院及合肥大科学中心的基金资助。
(合肥微尺度物质科学国家研究中心、生命科学学院)



 网站二维码
网站二维码  关注我们
关注我们 